Щороку 12 мільйонів людей у всьому світі переносять інсульт; багато хто вмирає або залишається інвалідами. В цей час для розчинення тромбу, що закорковує кровоносну судину, призначають препарати. Ці препарати поширюються по всьому організму, тому для досягнення тромбу потрібна висока доза. Це може спричинити серйозні побічні ефекти, такі як внутрішня кровотеча. Оскільки ліки часто потрібні лише в певних ділянках тіла, медичні дослідження вже давно шукають спосіб використання мікророботів для доставлення ліків туди, де вони необхідні: у разі інсульту – безпосередньо до тромбу, що утворився в результаті інсульту. Група дослідників зі Швейцарської вищої технічної школи Цюриха (ETH Zurich) досягла значних проривів на кількох рівнях. Результати дослідження опубліковано в журналі Science.
Потрібні високоточні наночастинки
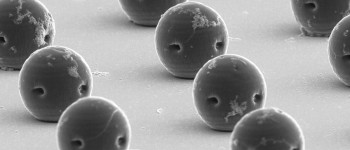
Мікроробот, що використовується дослідниками, є запатентованою сферичною капсулою з розчинної гелевої оболонки, якою можна керувати за допомогою магнітів і яка направляє препарат в організм до місця призначення. Магнітні властивості капсули забезпечують наночастинки оксиду заліза. «Оскільки судини в людському мозку вкрай малі, існує обмеження на розмір капсули. Технічне завдання полягає в тому, щоб гарантувати, що така маленька капсула також має достатні магнітні властивості», — пояснює Фабіан Ландерс, провідний автор статті та науковий співробітник Лабораторії багатомасштабної робототехніки ETH Zurich.
Мікророботу також необхідний контрастний агент, щоб лікарі могли відстежувати його переміщення судинами за допомогою рентгенівських променів. Дослідники зосередилися на наночастинках танталу, які широко використовуються в медицині, але складніше контролювати через їх більшу щільність і вагу. «Об'єднання магнітних властивостей, візуалізації та точного управління в одному мікророботі зажадало ідеальної взаємодії між матеріалознавством та робототехнікою, на досягнення якої у нас пішли роки», — каже професор ETH Zurich Бредлі Нельсон, який десятиліттями займається дослідженнями мікророботів. Професор Сальвадор Пане, хімік з Інституту робототехніки та інтелектуальних систем, та його команда розробили прецизійні наночастинки оксиду заліза, які забезпечують цей тонкий баланс.
Спеціальний катетер вивільняє капсулу із ліками
Мікророботи містять активний інгредієнт, необхідний для доставлення. Дослідники успішно завантажили мікророботів поширеними лікарськими препаратами для різних застосувань – у цьому випадку тромборозчинним засобом, антибіотиком або протипухлинним препаратом. Ці препарати вивільнялися високочастотним магнітним полем, яке нагрівало магнітні наночастинки, розчиняючи гелеву оболонку мікроробота.
Дослідники використовували двоетапну стратегію для наближення мікроробота до мети: спочатку вводили мікроробота в кров або спинномозкову рідину через катетер. Потім вони використовували електромагнітну навігаційну систему направлення магнітного мікроробота до мети. Конструкція катетера заснована на комерційно доступній моделі з внутрішнім провідником, з'єднаним із гнучким полімерним захопленням. При просуванні за межі зовнішнього напрямного пристрою полімерне захоплення розкривається та звільняє мікроробота.
Для точного управління мікророботами дослідники розробили модульну електромагнітну навігаційну систему, що підходить для використання в операційній. «Швидкість кровотоку в артеріальній системі людини сильно варіюється залежно від місця розташування. Це робить навігацію мікроробота дуже складною», – пояснює Нельсон. Дослідники об'єднали три різні стратегії магнітної навігації, що дозволило їм здійснювати навігацію на всіх ділянках артерій голови.
Це дозволяє їм котити капсулу вздовж стінки судини за допомогою магнітного поля, що обертається. Капсулу можна направляти до мети з неймовірною точністю зі швидкістю 4 міліметри на секунду.
В іншій моделі капсула переміщається за допомогою градієнта магнітного поля: в одному місці магнітне поле сильніше, ніж в іншому. Це притягує мікроробота в судині до сильнішого поля. Капсула може навіть рухатися проти течії — зі значною швидкістю потоку понад 20 сантиметрів за секунду. «Дивно, скільки крові протікає нашими судинами з такою високою швидкістю. Наша навігаційна система має бути здатною витримати все це», — каже Ландерс.
Коли мікроробот досягає складної для маневру ділянки розгалуження судини, набуває чинності система навігації по потоку. Магнітний градієнт направлений до стінки таким чином, що капсула потрапляє у потрібну судину.
Поєднуючи ці три стратегії навігації, дослідники отримують ефективний контроль над мікророботами за різних умов кровотоку та анатомічних особливостей. Більш ніж у 95% випадків капсула успішно доставляла ліки у потрібне місце. "Магнітні поля і градієнти ідеально підходять для малоінвазивних процедур, оскільки вони проникають глибоко в організм і - принаймні при використовуваних нами рівнях і частотах - не надають на нього негативного впливу", - пояснює Нельсон.
Інновації не обмежуються робототехнікою
Для тестування мікророботів та їх навігації в умовах, наближених до реальних, дослідники розробили силіконові моделі, які точно відтворюють судини пацієнтів і тварин. Ці моделі судин настільки реалістичні, що тепер використовуються у медичному навчанні та продаються компанією Swiss Vascular, дочірньою компанією ETH. «Ці моделі є вкрай важливими для нас, оскільки ми багато практикувалися, щоб оптимізувати стратегію та її компоненти. З тваринами це неможливо», — пояснює Пане. У моделі дослідники змогли виявити та розчинити тромб.
Після численних успішних випробувань на моделі команда прагнула продемонструвати можливості мікроробота у реальних клінічних умовах. По-перше, їм вдалося продемонструвати на свинях працездатність всіх трьох методів навігації та те, що мікроробот залишається чітко видимим протягом усієї процедури. По-друге, вони провели мікроробота через мозкову рідину вівці. Ландерс особливо задоволений: «Це складне анатомічне середовище має величезний потенціал для подальших терапевтичних втручань, тому ми були такі раді, що мікроробот зміг знайти свій шлях і в цьому середовищі».
Застосування за межами судинних оклюзій
Крім лікування тромбозів, ці нові мікророботи можуть використовуватися при локальних інфекціях або на пухлинах. На кожному етапі розробки дослідницька група незмінно прагнула досягти своєї мети: забезпечити якнайшвидшу готовність всього створеного ними продукту до використання в операційних. Наступна мета — якнайшвидше розпочати клінічні випробування на людях. Говорячи про те, що мотивує всю команду, Ландерс каже: «Лікарі вже роблять неймовірну роботу в лікарнях. Нас надихає усвідомлення того, що ми маємо технологію, яка дозволяє нам допомагати пацієнтам швидше та ефективніше, а також дарувати їм нову надію завдяки інноваційним методам лікування».